���A��W(xu��)���͏��ý����n�}�M: �������ļ�ǻ�ҵĹ��̻���(g��u)�������M(j��n)չ(2)
�r(sh��)�g��2022-01-18 14:41 ��Դ�������ӡ�������� ���ߣ�admin ��x����
������K�еķ�Ѫ��ϵ�y(t��ng)������(d��ng)�}��С��(d��ng)�}���o�}��С�o�}��ë��(x��)Ѫ�ܣ�ֱ����Խ�ׂ�(g��)��(sh��)����(j��)������(n��i)Ƥ��(n��i)�Ӻͻ���Ĥ����⣬�߶�ë��(x��)Ѫ��߀ϡ��ر���Ƥ��(x��)�����w�����г߶�С��(d��ng)�}�ʹ�߶Ȅ�(d��ng)�}�t��ƽ������(x��)���Լ����Ե����zԭ�w�S�Y(ji��)�ϡ�ë��(x��)Ѫ���ڴ�s200 ��m�ľ��x��(n��i)�錍(sh��)�|(zh��)��(x��)���ṩ��Ч�ĠI(y��ng)�B(y��ng)�����⽻�Q���������(d��ng)�}��С��(d��ng)�}������ѪҺ�IJ���(d��ng)����(d��ng)(�D4a)����Ŀǰ��ֹ���о��ˆT�ڹ��̽M����Ѫ�ܺ��г߶�Ѫ�ܵ��γɷ���քeȡ���˺ܴ��M(j��n)չ(�D4b-f)����(n��i)Ƥ��(x��)�������d��(x��)�����|(zh��)���ԽM�b�γ��߶�ë��(x��)Ѫ�ܣ�Ȼ�����������y�����w���ע�����w��(n��i)�c����Ѫ�����Ǻϡ����﹤�̷��������ɔ�(sh��)��������(sh��)�����г߶�Ѫ�ܣ����c����Ѫ�ܽY(ji��)�ϣ�Ȼ������������Ч�،��I(y��ng)�B(y��ng)���|(zh��)ݔ�͵��܇��M������ˣ���߶�ECP���L(zh��ng)��������Ҫ���w���γ����г߶�Ѫ�ܣ�ģ�M��(f��)�s�Ķ�߶�Ѫ�ܡ�

�D4
�˷��U(ku��)ɢ���Ƶ�Ѫ�ܻ����ԡ��߶�ë��(x��)Ѫ��(b-d)���г߶�Ѫ��(e-f)���w���γ��Ǻ����K�M��������ģ��߶�ë��(x��)Ѫ�ܵ��w���γ���ه�ڃ�(n��i)Ƥ��(x��)��(EC)���ԽM�b������Ѫ��������Ѫ���γ��(q��)��(d��ng)(b)��Ѫ��ȡ������?f��)�Y(ji��)��(g��u)�ؽ������W(xu��)��̖(h��o)�{(di��o)��(ji��)(c)��ͨ�^������Ƥ��(x��)�����ṩ���m�����W(xu��)�h(hu��n)�����M(j��n)Ѫ�ܳ���(d)���Ό�Ѫ�ܵ��γ���ͨ�^��Ѫ�ܼ�(x��)�����ڕr(sh��)�a(ch��n)���A(y��)�Ș�(bi��o)ӛ��ͨ������EC���N���γɵ�(e)��ͨ�^ͬ�S��ӡ�͔U(ku��)ɢ�T��(d��o)���z�������γɶ��Ӯ��|(zh��)Ѫ��(�Df)��

�D5
���̻��ļ��M�����߶ȡ��г߶�Ѫ�ܘ�(g��u)����������(n��i)Ƥ��(x��)��(EC)�܉��ԽM�b��ë��(x��)Ѫ�ܽY(ji��)��(g��u)���Ƀ�(n��i)Ƥ��(x��)���خ���PECAM-A(�Gɫ)��DAPI(�{(l��n)ɫ)Ⱦɫ(a)��EC��VEGF�ݶ�(�tɫ���^)���Ȱl(f��)���zԭ֧�ܣ������_����-���P�h(hu��n)��(�Sɫ)��DAPI(�{(l��n)ɫ)Ⱦɫ����ɫ�͟oɫ���^�քe��ʾ�c�o��(x��)�����B�ͷ��x�ļ�˼�(x��)��(b)���C(j��)е�s���l�����w�S�������z��ë��(x��)��ȡ��(n��i)Ƥ��(x��)���ɼtɫ
hCD31��(bi��o)ӛ���D(zhu��n)��(d��o)��Ƥ��(x��)���ɾGɫ�ɹ⵰��(GFP)��(bi��o)ӛ����(x��)�������{(l��n)ɫHoescht��(bi��o)ӛ(c)���cGelMAˮ���z�е�Ѫ���܇���(x��)�������B(y��ng)���M(j��n)ë��(x��)Ѫ�ܵij���ͷ�(w��n)�������Ѓ�(n��i)Ƥ��(x��)����DsRed��(bi��o)ӛ�����_(d��)��SMA��ƽ������(x��)�����g���|(zh��)�ɼ�(x��)���ֻ�����(d)��ͨ�^���ӽM�b�����A(y��)���O(sh��)Ӌ(j��)��?f��)�Y(ji��)��(g��u)�ؽ��Π���zԭˮ���z���γɿɹ�עѪ��ͨ������(n��i)Ƥ��(x��)����CD31(�tɫ)��DAPI(�{(l��n)ɫ)Ⱦɫ(e)����3D��ӡ������׃��Pluronic
F127ģ���ϝ��T�d��(x��)��ˮ���z�γɿɹ�עѪ��ͨ����ͨ����(n��i)��HUVEC(�tɫ)�r��܇��M�������������������Ƥ���w�S��(x��)��(HNDFs���Gɫ)(f)��ʹ���d��EC�Ġ�������īˮ3D��ӡ�w�S��ͨ�^������ӡ�ķ�������Ѫ�ܻ����K�ļ��a(b��)Ƭ����CD31(�Gɫ)�ͼ���(d��ng)����(�ۼtɫ)Ⱦɫ(g)��ͨ�^������ӡ�����γ�Ѫ��ͨ��������HUVECs(�Gɫ)��ע(h)����DMD���w��̷�ֱ������Ѫ�ܻ��M����HUVEC(�tɫ)���b��ͨ���У�HepG2��(x��)��(�Gɫ)���b���܇��M����(i)�����ù��г��ķ����ڟɹ������ˮ���z(�Gɫ)�����ɷ���Ѫ��ͨ�������ßɹ���(�tɫ)��ע(j)��ͨ�^ͬ�S��ӡ�����γ��p��Ѫ��(�Dk)��
���̻��ļ�ǻ��(ECP)�ij���һ���棬�mȻ���켼�g(sh��)�e��3D��ӡ���g(sh��)�܉_���Ƽ�(x��)����������ϵĿ��g���e���Ԅ�(chu��ng)��ǻ�ҵ���?f��)�Y(ji��)��(g��u)�ؽ��Π�����̻��ļ�ǻ�Ҳ����Ԅ�(d��ng)�@����Ȼ���K�Ĺ��ܡ����̽M��ͨ����Ҫ��(j��ng)�^��(sh��)�ܻ�(sh��)�µ��w�����B(y��ng)��ͨ�^��(x��)��𤸽���M���ͻ��|(zh��)���e�ȷ�ʽ��ɽM���ΑB(t��i)�γɺͳ��졣��һ���棬���ܸɼ�(x��)���ij��F(xi��n)��������̥�ɼ�(x��)��(ESC)���T��(d��o)���ܸɼ�(x��)��(iPSC)�����w��a(ch��n)���ļ���(x��)��(CM)�ṩ����Ч�ļ�(x��)����Դ�����Ҿ����R��Ҏ(gu��)ģ�ĸ�ͨ�����ȡ�Ȼ�����ɼ�(x��)���ֻ����ļ���(x��)��(PSC-CM)ͨ���Dz�����ģ���Y(ji��)��(g��u)�������������̥���ļ���(x��)��(�s��ʮ����)����(x��)���ͽM��ˮƽ�ϵIJ��������ѽ�(j��ng)�O�����K�������ļ������еđ�(y��ng)�á����磬PSC-CM���������K�ļ��a(b��)Ƭ�����䪚(d��)���ġ����|(zh��)�Ե��տs���(d��ng)���ܸ�׃�����ļ���늂������Ķ���(d��o)������������ʧ���L(f��ng)�U(xi��n)�������ֹ��ͨ�^ģ�M���K�l(f��)���^���е��w��(n��i)�h(hu��n)�����ѽ�(j��ng)�_�l(f��)����N���ԁ����M(j��n)���K���̽M���Ĺ��ܳ���(�D6)�����Ļ����Ŀǰ���̻��ļ��M���ij�����ԣ�����(qi��ng)�{(di��o)������?c��)ڹ��̻��ļ�ǻ�ҳ����еĝ������á��mȻĿǰ�����(sh��)������Զ���ͨ�^���S���B(y��ng)ģ�͡��߶ȵ�����ٻ����K��(g��u)������C���ģ����@Щ��������cѪ�ܻ�������Y(ji��)�ϣ��Н����ڸ���߶��ϑ�(y��ng)���ڹ��̻��ļ�ǻ�ҵij��졣

�D6
ģ�M�w��(n��i)�h(hu��n)�����w�������ԡ���̥�����ڣ���̥���K�L(zh��ng)�������w��֮���γ����ļ��Ӻ��ă�(n��i)Ĥ�ӽM�ɵ��Ĺܣ�����֮�g�й�����ļ�(x��)������|(zh��)����̥�����ڣ��Ĺ�ͨ�^�ۯB�����D(zhu��n)�ɭh(hu��n)�����ڹڠ�Ѫ��ϵ�y(t��ng)�͂���(d��o)ϵ�y(t��ng)�_ʼ�l(f��)����ͬ�r(sh��)�D(zhu��n)׃?y��u)�ǻ�����K�����x��׃����(x��)������|(zh��)�ͷǼ���(x��)��������Լ��C(j��)е��늴̼��f(xi��)ͬ���ã����M(j��n)CM��δ����̥��������ȫ��������ڰl(f��)��(a)��hiPSC��Դ�Էֻ��܉�õ�����̶��c����̥��CM�ஔ(d��ng)hiPSC-CM��Ŀǰ�ѽ�����һ�״��M(j��n)���K���̽M���w���������﹤�̷����������L(zh��ng)�����B(y��ng)�������T��(d��o)���c�Ǽ���(x��)�������B(y��ng)����(x��)��-���|(zh��)����ú����������̼���(b)��
չ���c���Y(ji��)
���^ȥ�Ď�������Џ�(f��)�s��?f��)�Y(ji��)��(g��u)�ؽ����Եĺ��^ECP���Ƃ���Ժ��߶�ECT�ij������ȡ�����@�����M(j��n)չ���S���ɼ�(x��)����������Ϻ�3D�����ӡ�ȼ��g(sh��)�Ŀ��ٰl(f��)չ���ںϽ��棬�����Թ��̻��ļ�ǻ�ҵ��w������ȡ�����L(zh��ng)����M(j��n)�����������ӭ���������˹����K����ƪ�C��ӑՓ�˹����Թ��̻��ļ�ǻ�ҵ�һЩ��Ҫ����(zh��n)����Ҫƿ�i�����c���졢Ѫ�ܻ��ͳ������P(gu��n)�Ć��}����Q�@Щ����(zh��n)�����ںܴ�̶������M(j��n)���K�ޏ�(f��)�����K�������w�⽨ģ�ļ��g(sh��)ˮƽ�������@Щƿ�i�������P(gu��n)�I������(zh��n)����PSC-CM�ijɱ�Ч��ͺ��^�U(ku��)չ�������ļ��c�����ļ�������ϡ������C(j��)�w�������ų⡢�͜ر���ͱO(ji��n)���ϵK�ȣ���Ҫ��δ�����R���D(zhu��n)���м��Խ�Q��
�����īI(xi��n)
���ĵ�һ���ߞ����A��W(xu��)�C(j��)еϵ�����������ĵIJ�ʿ������ͨӍ���ߞ����A��W(xu��)�C(j��)еϵ�����������ĵ��������ڡ����ø��о��T��
Fang Y, Sun W, Zhang T, Xiong Z. Recent advances on bioengineering approaches for fabrication of functional engineered cardiac pumps: A review. Biomaterials 2022;280:121298.
https://doi.org/10.1016/j.biomaterials.2021.121298
(؟(z��)�ξ���admin)
��һƪ���Ͽƴ�CoCo���C�����B�m(x��)�w�S����(qi��ng)��(f��)�ϲ������������е��O(sh��)Ӌ(j��)�C(j��)���̈́�(chu��ng)��(y��ng)��
��һƪ����ؔ(c��i)��F(tu��n)�(du��)�о����R������ۏ�(f��)�����z����׃�W(xu��)��3D��ӡ���ܡ�
��һƪ����ؔ(c��i)��F(tu��n)�(du��)�о����R������ۏ�(f��)�����z����׃�W(xu��)��3D��ӡ���ܡ�
���P(gu��n)��(n��i)��
 ����(m��ng)����3D��ӡ����M����
����(m��ng)����3D��ӡ����M���� 16�q���������ִꡱ�ۯB��
16�q���������ִꡱ�ۯB�� 3D Systems ��(chu��ng)ʼ��Chuck H
3D Systems ��(chu��ng)ʼ��Chuck H �����AԺʿ�I(l��ng)㕽��O(sh��)�K�ݴ�
�����AԺʿ�I(l��ng)㕽��O(sh��)�K�ݴ� ��h���S�մɿ���(j��ng)���R����
��h���S�մɿ���(j��ng)���R���� ������Ї�(gu��)��������a(ch��n)�I(y��)
������Ї�(gu��)��������a(ch��n)�I(y��)
- ������(m��ng)����3D��ӡ����M�����١���ʿ����
- ��16�q���������ִꡱ�ۯB���֙C(j��)��3D��ӡ
- ��3D Systems ��(chu��ng)ʼ��Chuck Hull��(d��ng)�x����(gu��)
- �������AԺʿ�I(l��ng)㕽��O(sh��)�K�ݴ�W(xu��)���ٲ����c
- ����h���S�մɿ���(j��ng)���R�������I(y��)����(y��ng)����
- ��������Ї�(gu��)��������a(ch��n)�I(y��)�l(f��)չ��Ϥ�ߡ�
- �������꣺�������켼�g(sh��)�l(f��)չ��(d��ng)�B(t��i)����(gu��)Fr
- ����Թ⣺���������b��ɿ��ԙz�y(c��)�x����
����(n��i)��
- ������(m��ng)����3D��ӡ����M�����١���ʿ����
- ��16�q���������ִꡱ�ۯB���֙C(j��)��3D��ӡ
- ��3D Systems ��(chu��ng)ʼ��Chuck Hull��(d��ng)�x����(gu��)
- �������AԺʿ�I(l��ng)㕽��O(sh��)�K�ݴ�W(xu��)���ٲ����c
- ����h���S�մɿ���(j��ng)���R�������I(y��)����(y��ng)����
- ��������Ї�(gu��)��������a(ch��n)�I(y��)�l(f��)չ��Ϥ�ߡ�
- �������꣺�������켼�g(sh��)�l(f��)չ��(d��ng)�B(t��i)����(gu��)Fr
- ����Թ⣺���������b��ɿ��ԙz�y(c��)�x����
- �����q���������������b���|(zh��)���ɿ���̽��
- ������⣺����3D��ӡ�ڹǿ��еđ�(y��ng)��
���]��(n��i)��
���c(di��n)��(n��i)��
- ����������r(sh��)���˳���3D��ӡ��δ������
- �����l(w��i)�tԺʿ�F(tu��n)�(du��)����������ܱ��ژ�(g��u)����
- �����A��W(xu��)Ҧ�W(xu��)�h���ڈF(tu��n)�(du��)��3D��ӡ�B�m(x��)�w
- �����L���h��(chu��ng)ʼ��Ҧ־�h����3D��ӡ�a(ch��n)Ʒ��
- ������Ƽ�������x���ʡ����֧Ӌ(j��)�����Ƽ�
- ��������Ժʿ�F(tu��n)�(du��)������ʽ��������ϥ�P(gu��n)��(ji��)
- ���Ͽƴ�CoCo���C�����B�m(x��)�w�S����(qi��ng)��(f��)��
- ������(gu��)��܊����(zh��n)���L(zh��ng)��3D��ӡ�������
- ����(gu��)���Ƽ���W(xu��)������Ⱥ��3D��ӡ��܊��(y��ng)
- ����h���S�մɿ���(j��ng)���R�������I(y��)����(y��ng)����


 �п�Ժ���ΈF(tu��n)�(du��)To
�п�Ժ���ΈF(tu��n)�(du��)To ���L���h��(chu��ng)ʼ��Ҧ
���L���h��(chu��ng)ʼ��Ҧ �㽭��W(xu��)�R������
�㽭��W(xu��)�R������ �����w���^(q��)�K朼�
�����w���^(q��)�K朼�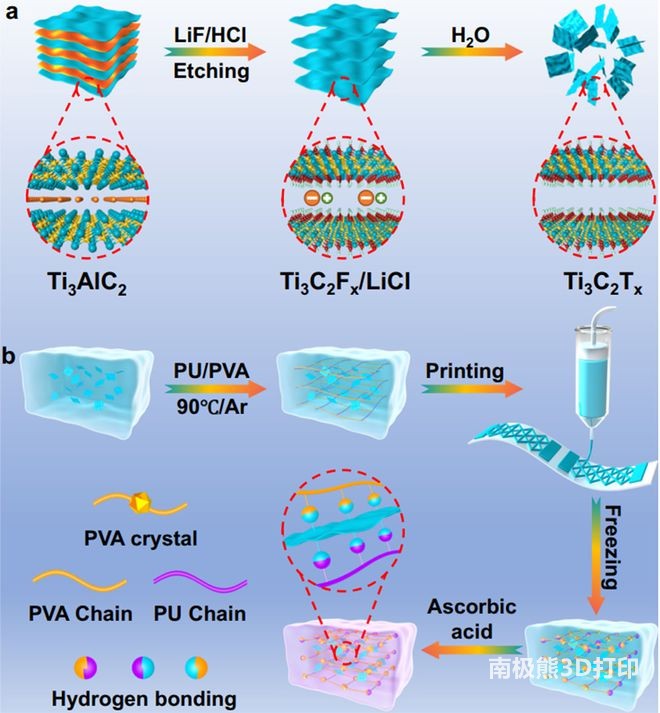 �S�SԺʿ�F(tu��n)�(du��)��3D
�S�SԺʿ�F(tu��n)�(du��)��3D �O��ݽ��ڣ��߷�
�O��ݽ��ڣ��߷�

