3D��ӡ�� - ˮ���z֧��ģ�M�Ĵ��M�������е�����֧���ޏ�
�������������^���У�����֧�����P��Ҫ�����ǽM���������W�j�ؽ��������𣬌��³ɹ����ޡ������L���ӣ�NGF���ڹ���������������֧�䣬���ΑB�l�����ף�BMPs���ڹ������^���г��m���_���T���ɹǷֻ�������Ȼ���L���Ӵ��ڷ����Բ�����ߡ��ɱ��ߵȆ��}�����I�B�����c�ɹ����P���L���ӵij��m���f�ͼ����{�ع������ęC���о��^�١�
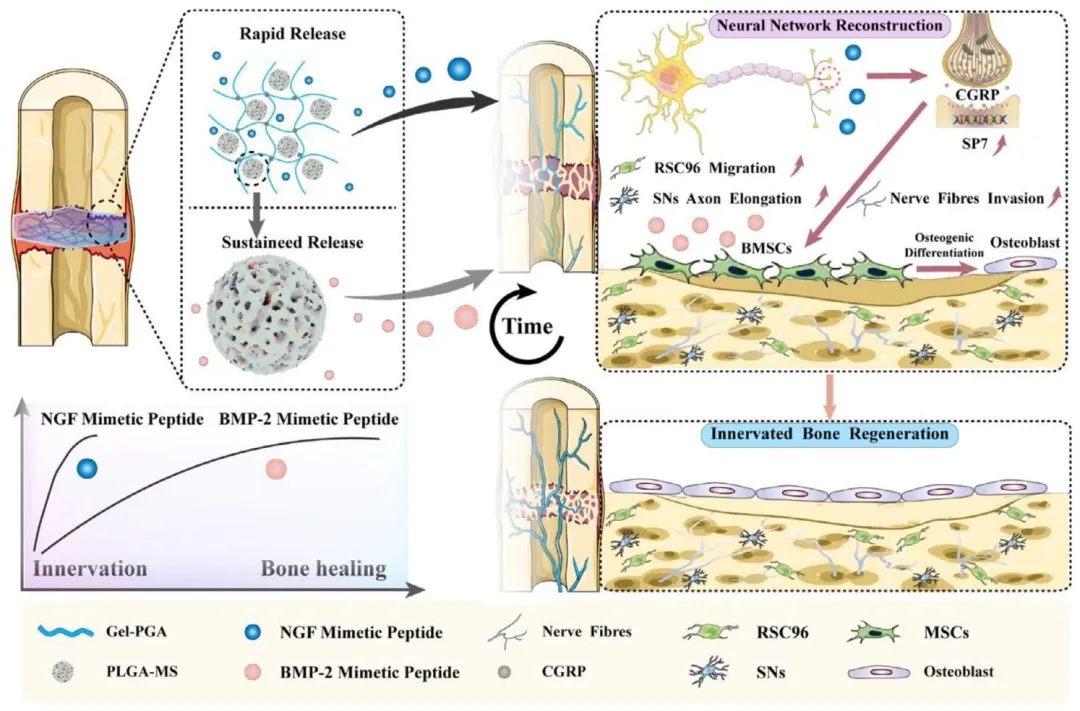
������ɽ��W����У�^�����t�W���̌WԺ�ď������ڈF��c�Ϸ��t�ƴ�W�����о����ĵ����������ڈF������OӋ��������һ�N3D��ӡ��-ˮ���z֧�ܣ�ͨ�^������-�u�����Ṳ���PLGA�������BMP-2ģ�M�ġ�ˮ���z���|ؓ�dNGFģ�M�ģ����F��NGFģ�M�ĵĿ���ጷź�BMP-2ģ�M�ĵ��L�ھ�ጡ�ԓ֧��ͨ�^�ɾ���ጷ����L����ģ�M�ģ����M�W�j�ؽ���������������̽������-�Ǵ��_�ķ��әC�ơ����P������“3D Printed Microsphere�Hydrogel Scaffold Facilitates Restoration of Reinnervation in Bone Regeneration through Programmable Release of NGF/BMP-2 Mimetic Peptides”���}�l���ڡ�Advanced Healthcare Materials���ϡ�

�����
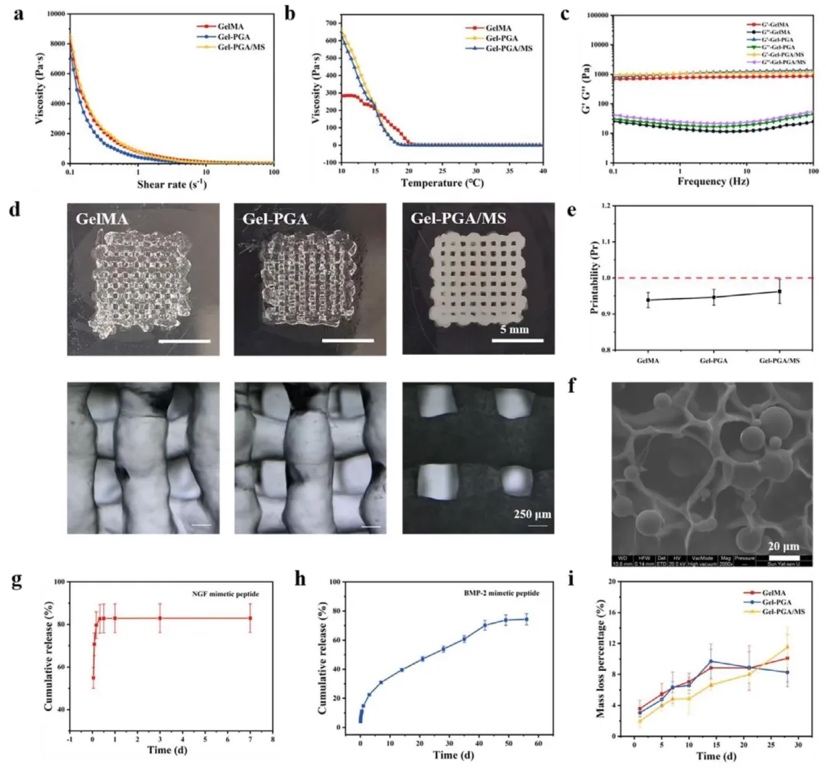
1. īˮ��׃�����c֧�ܱ�����ͨ�^��׃�yԇ���������ʡ��ضȡ��l�ʌ�ճ�ȼ�ģ����Ӱ푣�����������@�R��SEM���^�졢ጷ������y�������W���ܜyԇ�ȷ������о��˺�GelMA��mPGA��PLGA��Ĵ�ӡīˮ���Լ�3D��ӡ֧�����ܡ��Y��������īˮ�ʷ�ţ�D���w����׃ϡ���ԣ�20°C�rճ���m�˴�ӡ��֧�ܽY����������϶������PLGA������ɢ�ڽz���У�NGFģ�M��3����Ӌጷ�82.94±6.75%��BMP-2ģ�M��ͨ�^��-ˮ���z�o����Ì��F8��74.31±3.86%���mጷţ����s���Ⱥ��[Û�ʷքe�_����ˮƽ��4��ˮ��ʧ�ؼs11.51±2.58%��
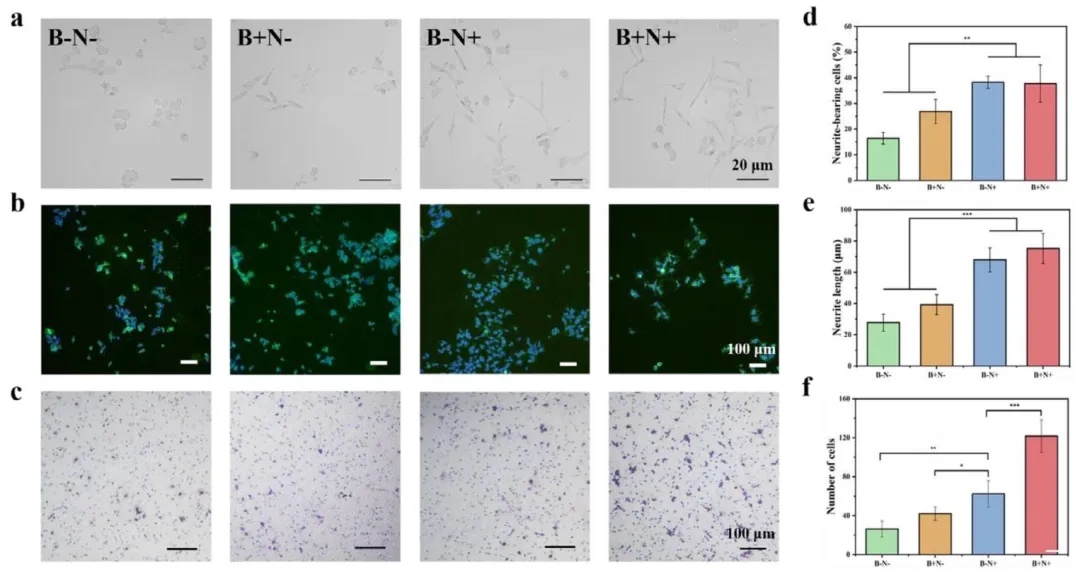
2. �w���ֻ����� ͨ�^PC12�������I�������t��������������ͻ�ֻ�Ⱦɫ��RSC96������ʩ�f������Transwell�w�ƌ����ߟɹⶨ���������о���֧����ȡ����������á��Y���@ʾ����NGFģ�M�ĵ�B-N+��B+N+�M�T��PC12�����γ��L�Sͻ����ͻ�L���@�����ӣ�����ͻ��Լ�������������B+N+�MRSC96�����w�Ɣ�����࣬�C��NGFģ�M�Ŀ���ጷſɼ����W�j�γɣ�BMP-2ģ�M�����Ѕfͬ���M���á�
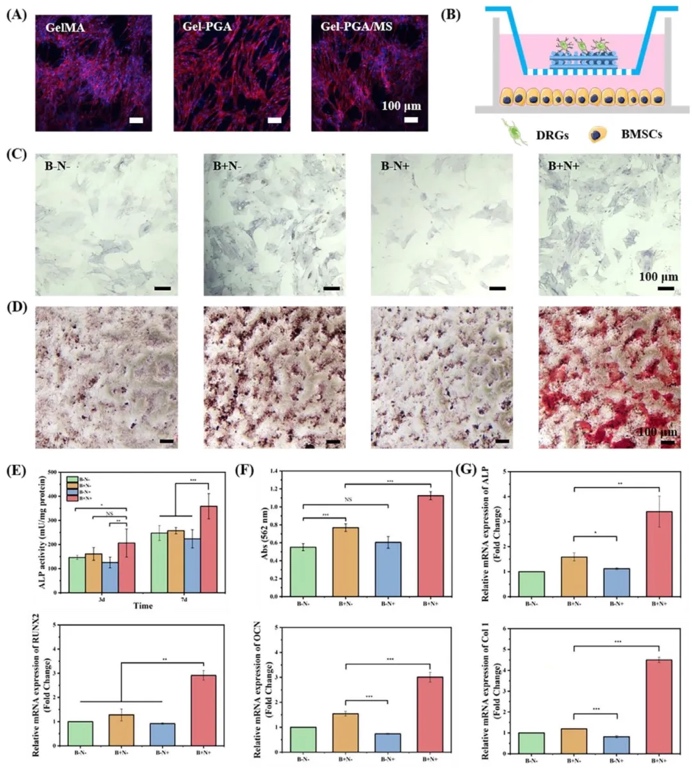
3. �w��ɹǷֻ����� ͨ�^BMSCs�cDRGs���������������B�wϵ���Y��ALPȾɫ�����ؼt�V���Y��Ⱦɫ��RT-qPCR�z�y���о���֧�܌��ɹǷֻ���Ӱ푡��Y��������B+N+�MALP������ߣ��}�Y�����e���@�����������M���ɹǻ���ALP��OCN��Col I���_ˮƽ���{������هCGRP�����}�ػ������P�ģ��錧��AMPK-CREB1��̖ͨ·����RUNX2���_��Ҫ��BMP-2ģ�M���{�ء�
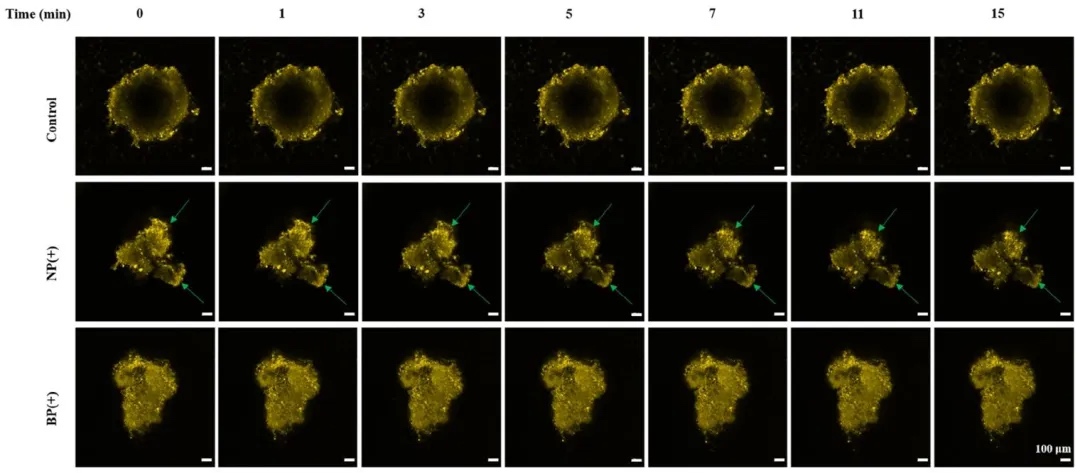
4. ͻ�|���ݰ���Ч������ ͨ�^FM1-43�ɹ��ӛDRGs�����������ȸ��X��Ԫ��ͻ�|���ݣ����r�^��NGFģ�M�Č����ݰ��µ�Ӱ푡��Y���@ʾ������NGFģ�M�ĺ�DRGs�ɹ⏊����3��犃��@���½�������ͻ�|����ጷ����ʼӿ죬��BMP-2ģ�M�Č����ݻ��ԟo���@Ӱ푡�ԓ����C��NGFģ�M��ͨ�^���M���f�|���ٷ��ڣ�������-�Ǵ��_��������̖������
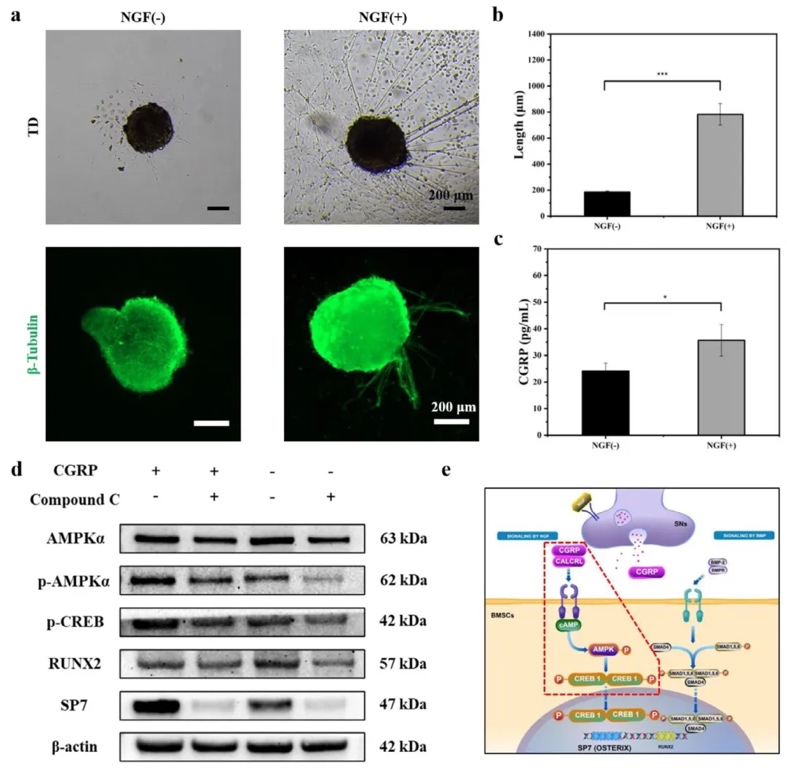
5. ��-�Ǵ��_���әC�� ͨ�^ELISA�z�yCGRP��ȡ�Western blotting������̖���ף��о���NGFģ�M���{�سɹǵęC�ơ��Y���@ʾ��NGFģ�M���@������DRGs���B������CGRP��ȣ�����AMPK��CREB1���ữ���M�����{�ɹ��D�����SP7������AMPK��Compound C̎���������ԓͨ·���C����ͨ�^CGRP-AMPK-CREB1-SP7�S���M�ɹǣ��cBMP-2ģ�M�ĵ�Smadͨ·�γɅfͬ��
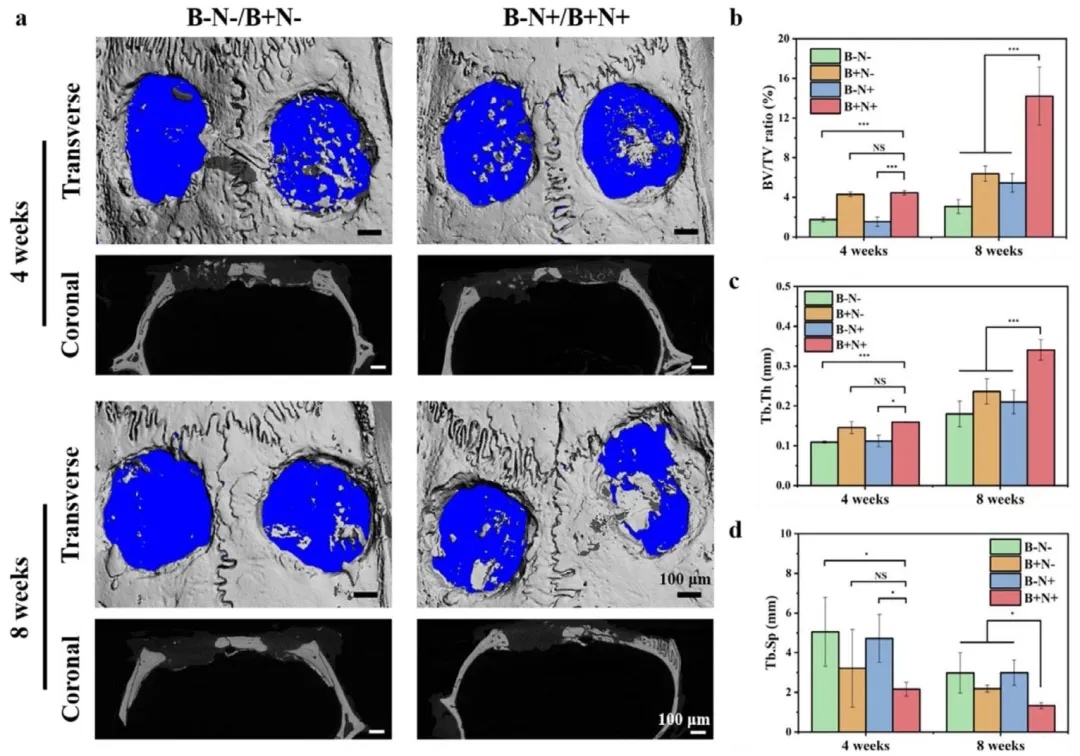
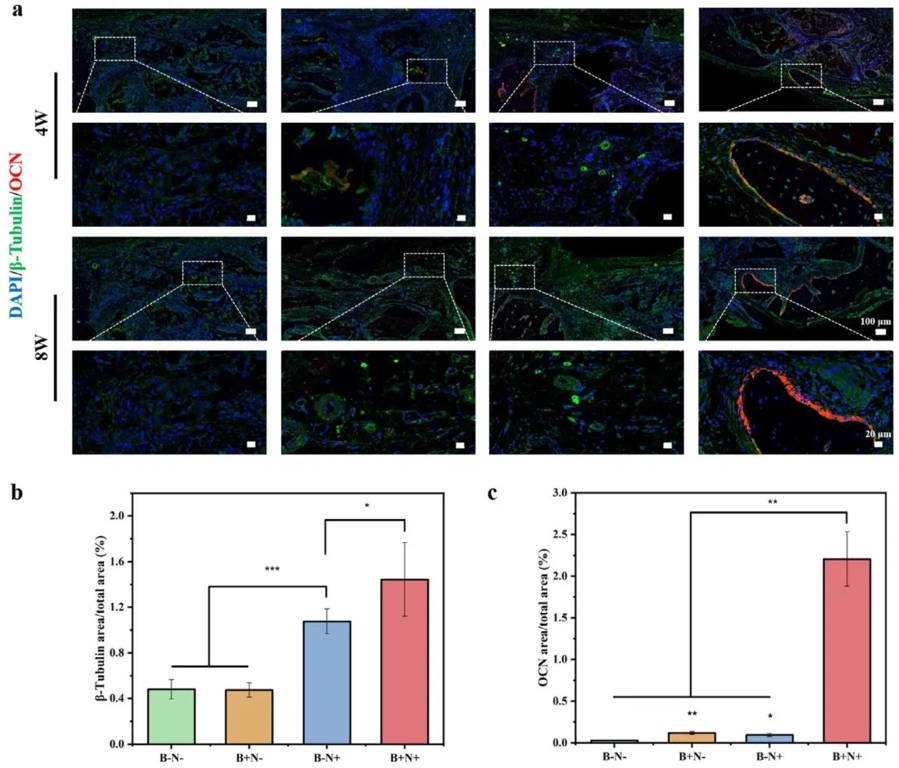
6. �w�ȹ������c����֧���u�� ͨ�^�����B��5mm�R��ȱ�pģ�ͣ��Y��Micro-CT���S�ؽ���H&EȾɫ��Masson��ɫȾɫ��β-tubulin/OCN���ߟɹ⣬�о���֧�ܵ��w�ȯ�Ч���Y���@ʾ��8�ܕrB+N+�MBV/TV�����w�e/���w�e����Tb.Th����С����ȣ���ߣ�Tb.Sp����С���g�ࣩ��С���������c���������Ͼo�ܣ�β-tubulin������w�S����ȱ�p���ģ�OCN��ԳɹDž^���@���U�����p���Ӆfͬ���M��-��������ϡ�
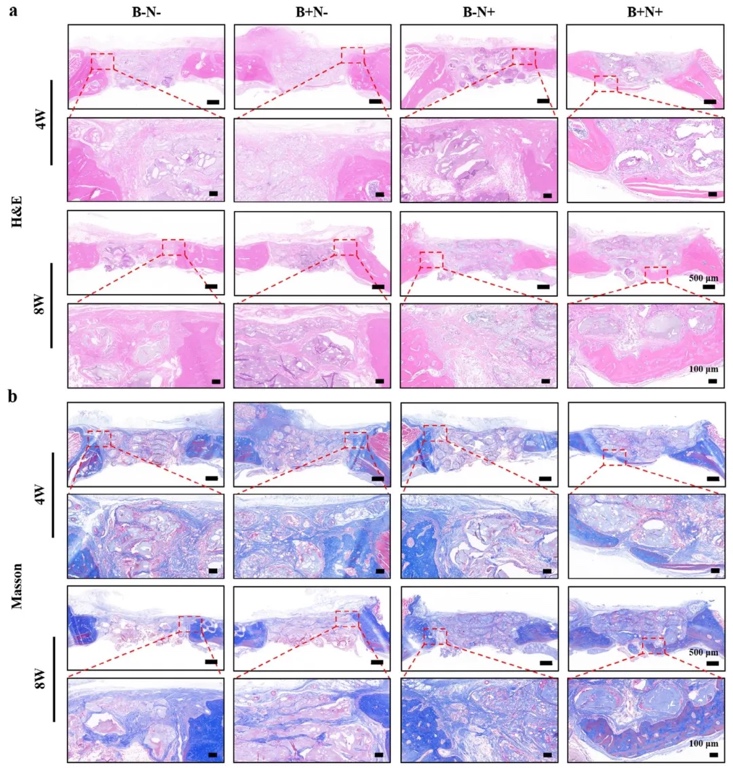
7. �M���W�c���ߟɹ���� ͨ�^H&EȾɫ�^���װY������MassonȾɫ�u���zԭ�w�S���ɼ�β-tubulin/OCN�p��Ⱦɫ��λ��-�ǽ��棬�о���֧�ܵ����������Ժ������h�����Y���@ʾ�����M���o���@�װY��B+N+�M8�ܕr��Ҋ���������zԭ�w�S��֧�ܿ�϶���У�β-tubulin������w�S�ܶ���ߣ�OCN��ԵV���^���wȱ�p���ģ���C������֧�䌦���������������á�
8. ���c�����P���������� ͨ�^���ߟɹ�Ⱦɫ����β-tubulin����^���OCN��ԹǽM����e���о���֧�܌���-����ϵ��{��Ч�����Y��������B+N+�Mβ-tubulin�����e�^���սM���Ӽs2����OCN�����e����3�����ϣ��C��NGF/BMP-2ģ�M�Ĺ��f�Ϳ�ͬ���������w�S����ͳɹǻ��ԣ����F�����l���µĹ������h���ؽ���
�о��YՓ
���о��ɹ��OӋ��������һ�Nؓ�d�pNGF/BMP-2ģ�M�ĵ�3D��ӡ֧�ܡ��w�⌍������ԓ֧�ܿ���ጷŵ�NGFģ�M�Ŀɴ��MPC12�����ֻ���RSC96�����w�ƣ�ģ�M�˹����γ��^����NGF�ĕr��ጷ������������mጷŵ�BMP-2ģ�M�Ŀ���Ч���M�����g���|�ɼ����ɹǷֻ����C���о��l�F��NGFģ�M��ͨ�^����ͻ�|����ጷ�CGRP������AMPK-CREB1��̖ͨ·���cBMP-2ģ�M�ĵ�Smadͨ·�fͬ�����ɹǷֻ����w�Ȍ���C����ԓ֧�ܿɴ��M�������w�S����ȱ�p��λ���ؽ��W�j���M���@�������¹�����Ч�ʡ��C�ϣ����о��_�l��3D��ӡ��-ˮ���z֧��ͨ�^ģ�M��Ȼ���L���ӵĕr��ጷ�ģʽ����ǽM�����������������ṩ��һ�N��ǰ���IJ��ԡ�
����Դ��
https://doi.org/10.1002/adhm.202501594
(؟�ξ���admin)
��һƪ�������_���{������W�_�l���͆β�����̎����ˇ���ӿ�̼���x�ߜ��մɺϳ��ٶ�
- ��Progress Group�Ƴ�SPI���g���A�ƻ���
- ��ABS�������M�����I���������켼�g����
- �������_���{������W�_�l���͆β�����̎
- ��3D��ӡ�� - ˮ���z֧��ģ�M�Ĵ��M��
- ���m����/���ƴ����������⁺Ͻ���
- ��3D��ӡ����W�ܴa�i��������׃ɫ�c�Ҝ�
- ����ľ�܆��l����ʿ3D��ӡ�����ޏ��L����
- ��Wayland Additive 3D��ӡ⁺Ͻ�ِ܇��
- ��3Dͬ�S��ӡ߀ԭ����ʯīϩ�����z������
- ������ɣ��������W����AI����316L���P�
- ���������ӌW����ܵ���������TC4��ˇ��
- ���p���Ӿۺϡ��߾��������I��ġ����ǡ�
- ��3D��ӡ����Y���OӋ�K�Oָ�ϣ������p��
- ���C���������·���3D��ӡ���g
- ��3D�����ӡ���g����������ٹ����е���
- ���B�m�����̼��g����ͻ�ƣ�Carbon����
- ���u݆�~Ƭ�����������������ޏͼ��g����
- ���Gɫ�ְ�ȫ��3D��ӡ�zԭˮ���z���IJ���
- ���P�c2024��ʮƪ�l����Science��Nature
- ��3D��ӡ�C���g���ƴ��FDM��SLA��CLIP��


 Progress Group�Ƴ�SPI��
Progress Group�Ƴ�SPI�� ABS�������M�����I������
ABS�������M�����I������ �����_���{������W�_�l��
�����_���{������W�_�l�� �m����/���ƴ���������
�m����/���ƴ��������� 3D��ӡ����W�ܴa�i������
3D��ӡ����W�ܴa�i������ ͻ��������3D��ӡ
ͻ��������3D��ӡ �ϰ�LEAP 71��˾
�ϰ�LEAP 71��˾ 3D�����ӡ������
3D�����ӡ������ ��Small Science
��Small Science ��������-�����
��������-����� ���A��W��������
���A��W��������

