�AѪ�ܻ�������ٵ�3D�����ӡ���ڿ���ԭλ�B���ޏ��о��Mչ
�B��ȱ�p���������P�I�ߴ���B��ȱ�p���������������������ޣ��������ϕr�g�L����������ȫ���Dz��B�L�U�ߵȆ��}����ǰ�R���ޏ��ֶ������ֲ���ͬ�N���w��ֲ����˹���ֲ��ȣ����R���w���ޡ����ڼ��������L�U���ޏ�Ч������������𡣂��y�ǽM�����̵�“���϶���”�����������ӷN���������֧�ܣ����ڼ����ֲ��������I�B�Uɢ���㡢֧�ܽ������y��ȱ�ݣ����y�ԏ��ƹ������s�Y����ͬ�r�ɼ����ۼ��w�w��ɹ��T���r�g�L��Ѫ�ܻ����㣬�����˿���ԭλ�ɹǡ�
���Q�������}�����A��W���������n�}�M�c�����f���t�WԺ����n�}�M���������һ�N���Ͱl�����̲��ԣ����g���|�ɼ�����MSCs������Ě�o�}��Ƥ������HUVECs���c�ɹ��w���Y�ϣ���Ҏģ���������ԽM��Ѫ�ܻ��ͳɹ����Ե��AѪ�ܻ�������١��F�ϵ�y�Y�x��ʯīϩ�����GO��������ɹ��w������ͨ�^ճ���ߺ�PI3K/Aktͨ·�@�����M�ɹǷֻ����Mһ���������ؓ�d�����z����ϩ������GelMA��ˮ���z���M��3D�����ӡ���������и����ܶȺͳɹ������ď��s�M�������w���w�Ȍ���C����ԓ�����ɴ��M����Ѫ�ܻ��ǽM���γɣ����F�B��ȱ�p����Чԭλ�����ޏ͡�
���P������“3D Bioprinting of Prevascularized Bone Organoids for Rapid In Situ Cranial Bone Reconstruction”���}�l���ڡ�Advanced Healthcare Materials���ϡ������f���t�WԺ2022��������Ʋ�ʿ����溞��һ���ߣ����A��W�����ڡ������������ڼ��f���t�WԺ�����ڞ鹲ͬͨӍ���ߡ�

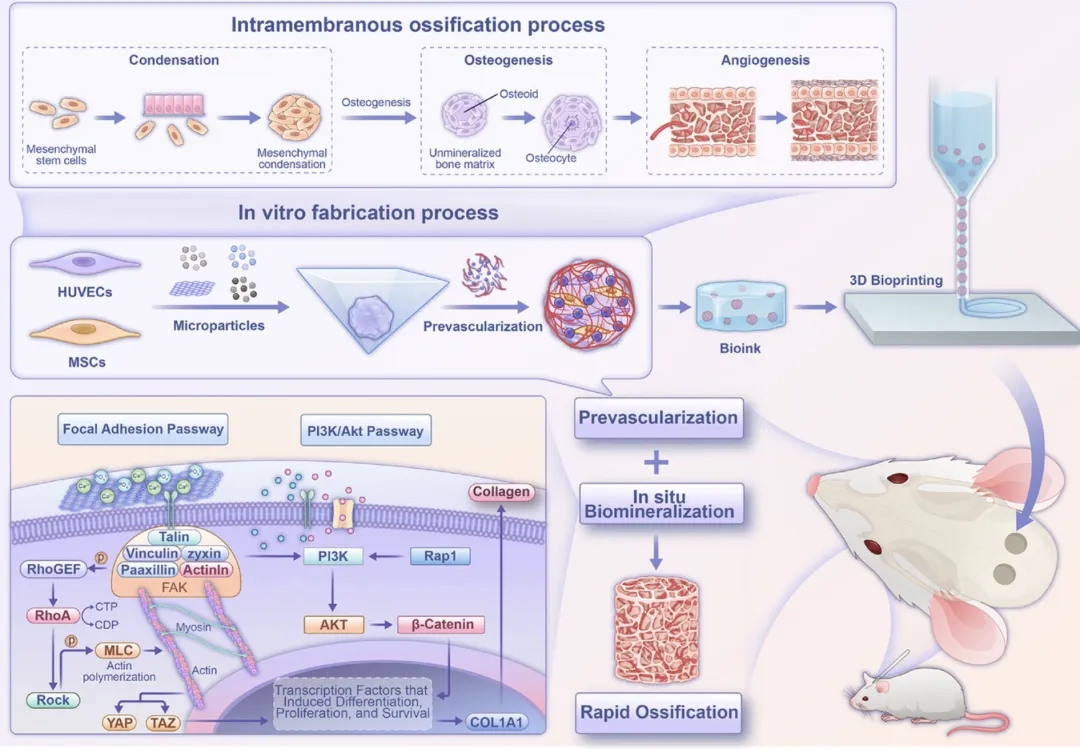
1. �о��OӋ�c�������ʾ��D��ͨ�^ʾ��Dչʾ�о����w�OӋ��������̣��о�������AѪ�ܻ�������ٵĘ����������B���ޏ��еđ��á��Y���������Y���g���|�ɼ�������Ƥ�����c�ɹ��w������ʯīϩ��������AѪ�ܻ�������٣���3D�����ӡ��ɴ��MԭλѪ�ܻ������������B��ȱ�p�ޏ��ṩ�²��ԡ�
2. �AѪ�ܻ��ɹǾۼ��w�ı����c���������Ï��ƾۼ����g�Ƃ京��ͬ�ɹ��w�����u����ʯ�����ﲣ����ʯīϩ������ȣ��ļ����ۼ��w��ͨ�^���r����PCR�����ߟɹ�Ⱦɫ�ȷ����u���ɹǻ�����_�c�������ԡ��Y��������ʯīϩ�����GO���M�ijɹ����P������ALP��COL-1��Runx-2�����_�@�����������M���Ҽ������������ã��C��GO���ɹǷֻ��Ĵ��M�������
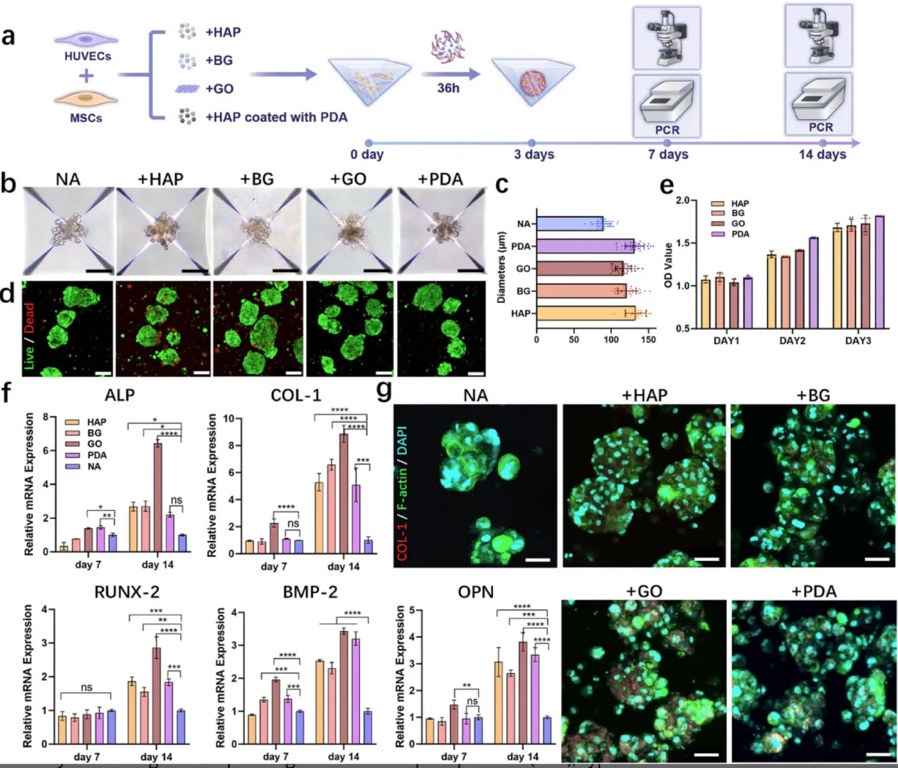
3. ؓ�dGO���AѪ�ܻ�������ٵijɹ��cѪ�ܻ��u�������ÉA������øȾɫ�����ؼtȾɫ��Ѫ�����Ɍ��о�GOؓ�d���AѪ�ܻ�������ٵijɹǵV�������cѪ�ܾW�j�γɡ��Y��������GO���M�}���e�c�ɹǷֻ����Һ���Ƥ�����ľۼ��w���ԽM���γ�ë��Ѫ�ܘӽY����CD31���_�C��Ѫ�ܻ��������f��ԓ����ټ�߳ɹ��cѪ�ܻ����ԡ�

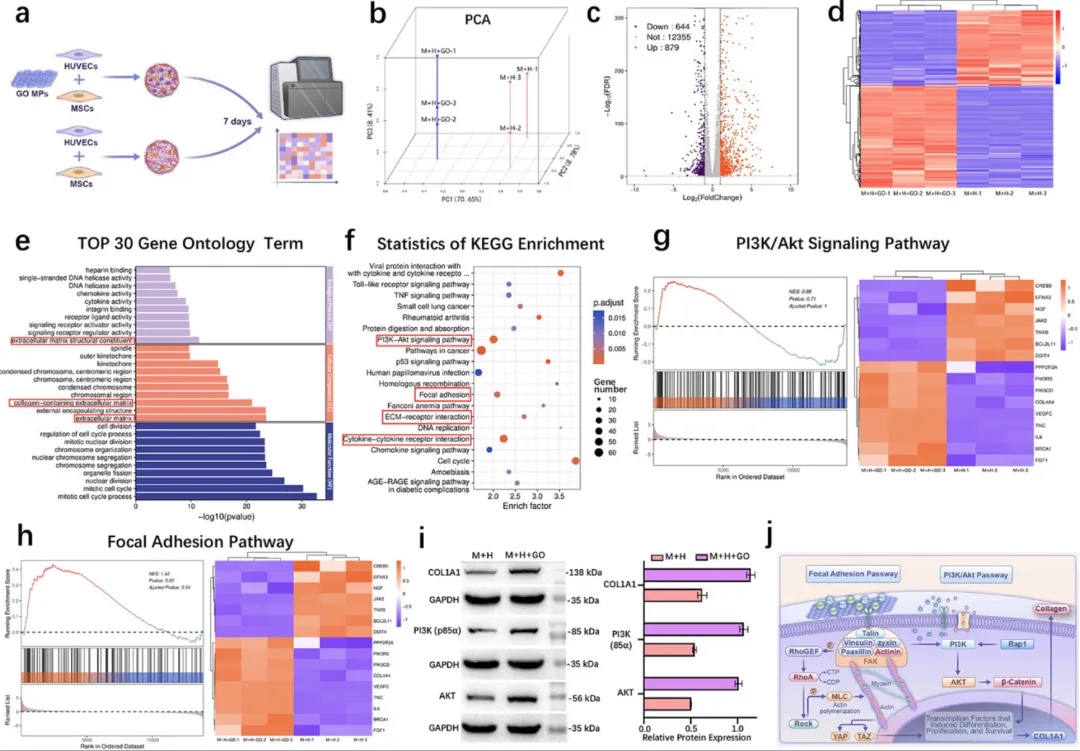
4. GO���M�ɹǷֻ��ķ��әC���D䛽M������ͨ�^mRNA�y���c������Ϣ�W�������о�GOӰ푳ɹǵķ���ͨ·���Y���@ʾ��GO�M����_������ճ���ߡ�PI3K/Akt��̖ͨ·�ȣ�Western blot��CPI3K��AKT�ȵ��ױ��_���{���C��GOͨ�^����ճ���ߺ�PI3K/Aktͨ·���M�ɹǷֻ��c��������|�ϳɡ�
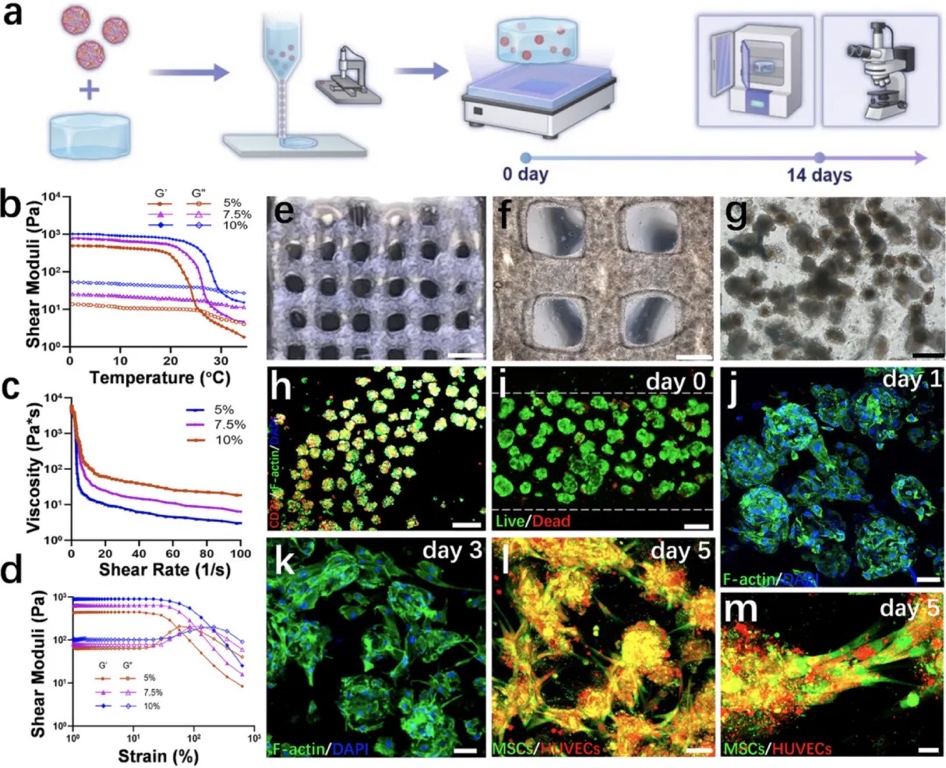
5. �AѪ�ܻ�������ٵ�3D�����ӡ��ˇ�c���ܡ��x��7.5 wt.% GelMAˮ���z��������īˮ�d�w��ͨ�^��׃�W�yԇ������ӡ�������Y�ϻ�/��Ⱦɫ�u������ viability���Y����������ӡ�Y���������õĔD���������c�������ԣ� viability ≈85.63%�����҃�Ƥ�������γ�Ѫ�ܾW�j���C��3D��ӡ���g�Ɍ��F����ٵ�Ҏģ�������c���ܱ�����
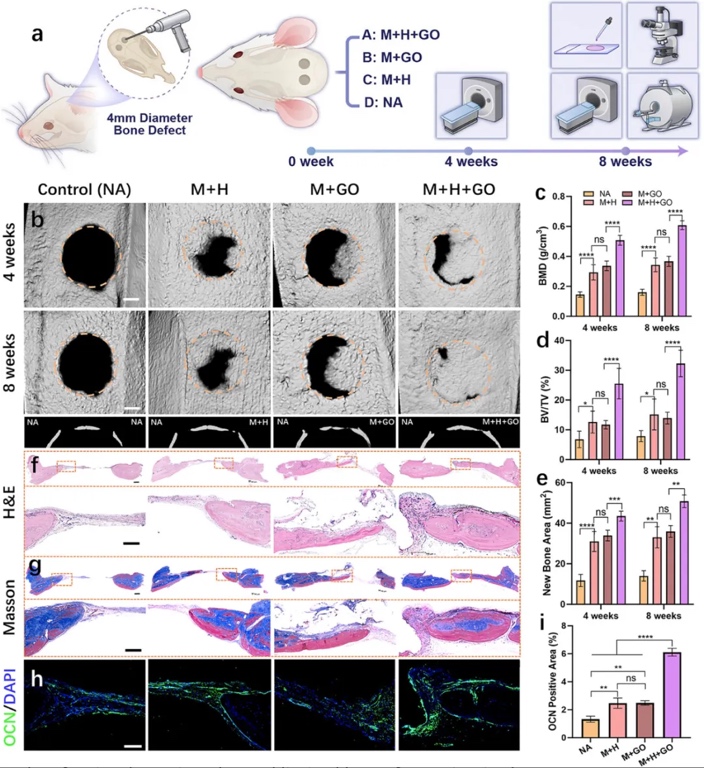
6. �B��ȱ�p�ޏ͵��w��Ч���u�����ڴ����B��ȱ�pģ����ֲ�벻ͬ̎���������ӡ construct��ͨ�^�@CT���M���WȾɫ��H&E��Masson��ɫ�������ߟɹ�Ⱦɫ�u���������cѪ�ܻ����Y����������GO�c��Ƥ�������AѪ�ܻ�������ٽM��M+H+GO���¹Ǹ��w�ʡ����w�e�֔���BV/TV=32.28±4.48%����Ѫ���ܶ��@�����������M���Ҵ��MM2�;��ɼ����O�����C�����Ч��ԭλ�������c����������
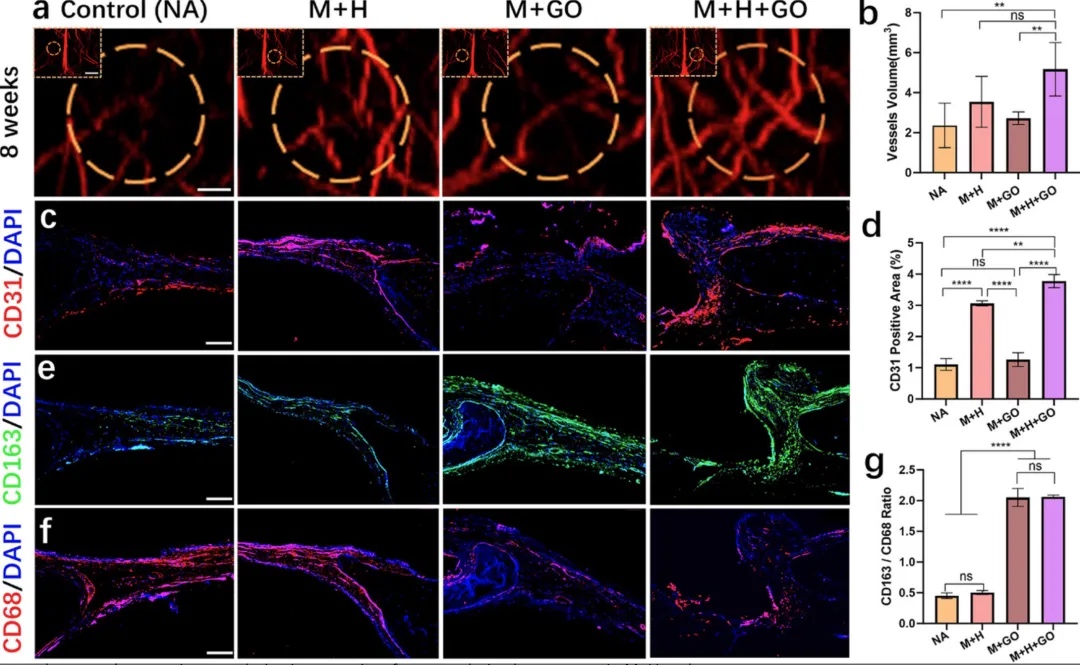
7. Ѫ�ܻ��c����푑��u�������ôŹ������MRI���c���ߟɹ�Ⱦɫ������ȱ�p�^���Ѫ�ܾW�j�γ��c���ɼ����O�����Y���@ʾ���AѪ�ܻ��M��M+H��M+H+GO��Ѫ���w�e�@�����ڌ��սM����GOؓ�d�MCD163+��M2�ͣ����ɼ����������ߣ������AѪ�ܻ��������ͨ�^����Ѫ�ܻ��c�����{�����M��������
�о��YՓ
���о����һ�N�Y���AѪ�ܻ���������c3D�����ӡ���²��ԣ����ڿ���ԭλ�B��������ͨ�^���g���|�ɼ�������Ƥ�����c�ɹ��w������ʯīϩ��������ϣ������˾����ԽM��Ѫ�ܻ������������ɹ����Ե�����١�3D�����ӡ���g�������ؓ�d��ˮ���z�У��γɶ��ƻ��Ĵ�����ֲ����F�˽ӽ����������ܶȵ�Ѫ�ܻ��ǽM���������w�Ȍ���@ʾ��ԓ����ͨ�^����ճ���ߺ�PI3K/Aktͨ·���M�ɹǷֻ�����ͨ�^��Ƥ�����ԽM�b�γ�Ѫ�ܾW�j���@�������B��ȱ�p��ԭλ���γɣ�ͬ�r�T��������M2���ɼ����O�����о��Y���������@�N�l�����̲��Կ˷��˂��y֧�ܷ����ľ����ԣ���������ṩ�˿ɔUչ����Ч;���������Ƅ���������ͽM���������R�������ί��еđ��á�
����Դ��
https://advanced.onlinelibrary.w ... 1002/adhm.202501376
(؟�ξ���admin)
- ��3D��ӡ���gͻ�ƣ����﹤���ȍu�����Π�
- ������3D��ӡ���F��ܛӲͨ�ԣ� - UT-Aust
- ���ؑc��W-ͬ����W-������W-��������
- ����3D��ӡ���M����ģ�;��������ɻ�
- ���AѪ�ܻ�������ٵ�3D�����ӡ���ڿ���
- ���O���˾�ͶӰ��̻��B�m3D��ӡ�����F��
- �� 3D��ӡ��500��ǰ��֫�֏���Ʒ��ʾ����
- ��Lithoz��LCM�մ�3D��ӡ��ν�Q�댧�w
- ��3D Systems�cTISSIUM�����@FDA���� ȫ
- ��Formlabs�cDMG MORI�ֲ����ձ��Ј���
- ���������ӌW����ܵ���������TC4��ˇ��
- ���p���Ӿۺϡ��߾��������I��ġ����ǡ�
- ��3D��ӡ����Y���OӋ�K�Oָ�ϣ������p��
- ���C���������·���3D��ӡ���g
- ��3D�����ӡ���g����������ٹ����е���
- ���B�m�����̼��g����ͻ�ƣ�Carbon����
- ���u݆�~Ƭ�����������������ޏͼ��g����
- ���Gɫ�ְ�ȫ��3D��ӡ�zԭˮ���z���IJ���
- ���P�c2024��ʮƪ�l����Science��Nature
- ��⁏��ˣ��K����3D��ӡ⁺Ͻ��q朣��b��


 3D��ӡ���gͻ�ƣ����﹤��
3D��ӡ���gͻ�ƣ����﹤�� ����3D��ӡ���F��ܛӲͨ��
����3D��ӡ���F��ܛӲͨ�� �ؑc��W-ͬ����W-������
�ؑc��W-ͬ����W-������ ��3D��ӡ���M����ģ��
��3D��ӡ���M����ģ�� �O���˾�ͶӰ��̻��B�m3D
�O���˾�ͶӰ��̻��B�m3D ͻ��������3D��ӡ
ͻ��������3D��ӡ �ϰ�LEAP 71��˾
�ϰ�LEAP 71��˾ 3D�����ӡ������
3D�����ӡ������ ��Small Science
��Small Science ��������-�����
��������-����� ���A��W��������
���A��W��������

